Formaldehyd – en viktig byggekloss i industrien
Aldehyder betegner en gruppe kjemiske forbindelser innenfor organisk kjemi der den funksjonelle gruppen består av karbon, hydrogen og oksygen (CHO). Formaldehyd er det enkleste av aldehydene, har lettgjenkjennelig lukt, og ble først oppdaget av Alexander Butlerov i 1859. Industriell framstilling av formaldehyd ble utviklet i løpet av 1900-tallet og molekylet har med sin høye reaktivitet og allsidighet fått en viktig plass som «byggekloss» i industrien.
Formaldehyd brukes til fremstilling av produkter som brukes av en rekke bransjer, inkludert bil-, luftfart-, kosmetikk- og legemiddelindustrien, og har spesielt stor betydning for trevirke som konstruksjonsmateriale gjennom finer-/sponplater og limtre.
Optimalisering for industrien
Industrielt fremstiller man formaldehyd fra metanol ved hjelp av en katalysator, enten sølv eller en blanding av metalloksider som jern og molybden. Den norske produsenten og teknologileverandøren Dynea AS på Lillestrøm finner størst forbedringspotensial i den sølvkatalyserte ruten, og KA Rasmussen AS framstiller slik katalysator på Hamar og selger denne til selskaper i mange land.
Oksidasjon av metanol til formaldehyd (MTF) over sølvkatalysator foregår ved nær atmosfærisk trykk, 600-700 °C og en fødemiks bestående av metanol, damp og luft reagerer til formaldehyd, CO2 og små mengder andre biprodukter. Selv om selektiviteten er relativt høy, dvs. 86-90% av metanolen reagerer til formaldehyd, så utgjør de 10-14 % som ikke omdannes eller i stedet danner CO2 et økonomisk og energimessig tap. Målet med mitt ph.d.-arbeid har derfor vært å se på om det er rom for å optimalisere formaldehydutbyttet i den sølvbaserte prosessen.
Lønnsom produksjon og redusert energiforbruk
Reaksjonen er utfordrende å studere blant annet fordi den foregår ved høy temperatur, og dette har begrenset den detaljerte forståelsen. Slike utfordringer har for andre reaksjonssystemer blitt løst i laboratoriet ved bruk av spesielle reaktorer med kort oppholdstid og sterk kontroll av temperatur og andre parametere. Ph.d.-arbeidet rapporterer for første gang en ringformet, såkalt annulær, reaktor benyttet for å studere MTF.
Den annulære reaktoren består av et sølvrør – katalysatoren – plassert inni et kvartsrør slik at reaktantene (molekylene som forbrukes i reaksjonen) strømmer raskt gjennom det trange sjiktet mellom dem. Dette gjør at vi undertrykker både reaksjoner i selve gassfasen og videre reaksjon av de produktene som først dannes på sølvoverflata.
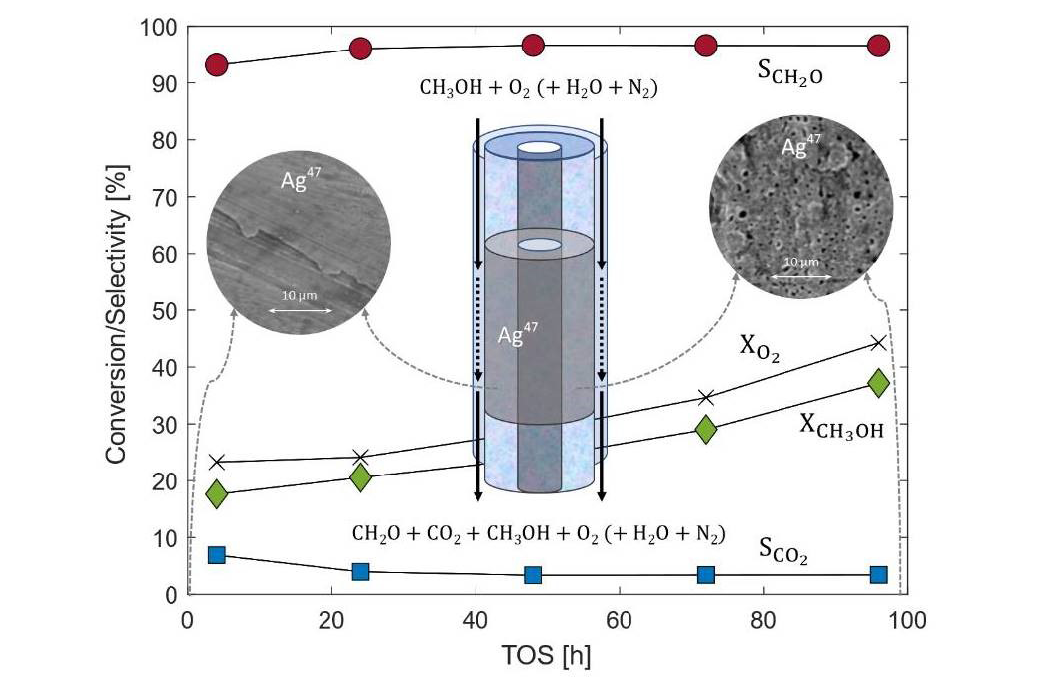
Dette har utvidet forståelsen rundt reaksjonene som foregår på sølvoverflata og en fagfellevurdering karakteriserte det som pionerarbeid. Fersk og brukt sølvkatalysator har også blitt undersøkt med elektronmikroskopi og røntgenstrålespreding for ytterligere å kartlegge hvordan de krystallinske egenskapene til sølvet påvirker reaksjonshastigheten, selektiviteten og levetida til katalysatoren.
I den annulære reaktoren oppnådde vi også selektiviteter på opp til 96% og vi ser derfor at vi kan oppnå en mer effektiv utnyttelse av råvaren metanol i MTF-prosessen. Når vi får utnyttet råvaren bedre reduseres energiforbruket og produksjonen blir mer lønnsom for bedriftene.
Dette viser hvordan grunnleggende kjemikunnskap kan være et viktig verktøy i forbedring av industrielle prosesser. At bedrifter kan oppnå lønnsom og energieffektiv produksjon er også en av forutsetningene til et grønnere og mer bærekraftig samfunn.
Veileder for doktorgraden har vært Professor Hilde J. Venvik

Stine Lervold
Stine Lervold var stipendiat ved Institutt for kjemisk prosessteknologi ved NTNU. Hun disputerte i mai 2021.
Search
Søk
Categories
- Arctic Research
- Arkitektur
- Bærekraft
- Bioingeniørfag
- Biologi
- Biology
- Biomedical Laboratory Science
- Biotechnology
- Bioteknologi
- Chemical Engineering
- Chemistry
- Climate
- Computer Science
- Datateknologi
- Digital
- Elektronikk
- Energi
- Energi
- Energy
- Engineering
- Engineering
- Environment
- Food Science
- Forskning
- Fysikk
- Fysikk
- Havbruk
- Informasjonsteknologi
- Informasjonsteknologi
- Ingeniørvitenskap
- Kjemi
- Kjemisk prosessteknologi
- Kjemisk prosessteknologi
- Kreftbehandling
- Kybernetikk
- Marine Technology
- Materialer
- Materials Science
- Materialteknologi
- Matvitenskap
- Meninger
- Miljø
- Min ph.d.
- My PhD
- My PhD
- My postdoc
- Nanotechnology
- Nanoteknologi
- Ocean
- Oil and gas
- Physics
- Research
- Simulering og visualisering
- Spør en forsker
- Studentliv
- Sustainability
- Ukategorisert
- Universitetsliv
- University Life
Kategorier
- Arctic Research
- Arkitektur
- Bærekraft
- Bioingeniørfag
- Biologi
- Biology
- Biomedical Laboratory Science
- Biotechnology
- Bioteknologi
- Chemical Engineering
- Chemistry
- Climate
- Computer Science
- Datateknologi
- Digital
- Elektronikk
- Energi
- Energi
- Energy
- Engineering
- Engineering
- Environment
- Food Science
- Forskning
- Fysikk
- Fysikk
- Havbruk
- Informasjonsteknologi
- Informasjonsteknologi
- Ingeniørvitenskap
- Kjemi
- Kjemisk prosessteknologi
- Kjemisk prosessteknologi
- Kreftbehandling
- Kybernetikk
- Marine Technology
- Materialer
- Materials Science
- Materialteknologi
- Matvitenskap
- Meninger
- Miljø
- Min ph.d.
- My PhD
- My PhD
- My postdoc
- Nanotechnology
- Nanoteknologi
- Ocean
- Oil and gas
- Physics
- Research
- Simulering og visualisering
- Spør en forsker
- Studentliv
- Sustainability
- Ukategorisert
- Universitetsliv
- University Life




